本文目录导航:
元素周期表分几个区块?
元素周期表是依据元素的原子结构和化学性质启动分区划分的。
经常出现的周期表分区包括主族元素、过渡元素、稀土元素和喷射性元素1. 主族元素(s-与p-区块):主族元素是周期表中IA至VIIIA族的元素,它们的最外层电子组态遵照s轨道和p轨道的填充规定。
主族元素通常具备相似的化学性质。
2. 过渡元素(d-区块):过渡元素位于周期表的IB至VIIIB族,它们的最外层电子填充在d轨道中。
过渡元素通常具备良好的金属个性,例如高导电性和可塑性。
3. 稀土元素(f-区块):稀土元素是周期表中镧系和锕系元素,它们的最外层电子填充在f轨道中。
稀土元素在化学性质上具备必定的相似性,同时也领有关键的运行价值。
4. 喷射性元素(喷射性区块):周期表的底部是喷射性元素区块,包括锕系元素和超铀元素。
这些元素的原子核不稳固,会出现喷射性衰变。
此外,周期表还可以经环节度行(期)和垂直列(族)启动划分。
水平行示意元素的能级壳层(横向电子排布),而垂直列示意元素的化学性质和周期性法令(纵向原子数参与),例如周期表中的同一族元素在化学性质上有相似之处。
总之,周期表的分区是依据元素的原子结构、最外层电子的填充规定以及化学性质等起因启动的划分。
这种划分有助于了解元素的个性和预测元素之间的相互作用。
为什么元素周期表要分区?
元素周期表的分区是依据元素的电子性能和化学性质启动划分的。以下是元素周期表的关键分区:
1.主族元素(或称为A族元素)
这些元素的最外层电子壳层蕴含 s 或 p 轨道的电子。
主族元素从第1族到第18族,共有8个主族元素区。
2. 过渡元素(或称为B族元素)
这些元素的最外层电子壳层蕴含 d 轨道的电子。
过渡元素通常指从第3周期到第12周期的元素。
3. 稀土元素(或称为内过渡元素)
这些元素的最外层电子壳层蕴含 f 轨道的电子。
稀土元素位于周期表的底部两行。
4. 杂类金属
这是一个蕴含一些不凡元素的分区,这些元素在化学性质上不属于主族元素或过渡元素。
5. 非金属元素
这些元素大少数状况下是气体或固体,在常温常压下不导电。
6. 碱金属和碱土金属
碱金属元素位于第1族,碱土金属元素位于第2族。
7. 卤素和气体元素
卤素元素位于第17族,气体元素(包括惰性气体)位于第18族。
此外,周期表还可以依照周期数和原子序数启动垂直划分。
周期数示意元素的电子壳层的数量,原子序数示意元素核中的质子数量。
元素周期表的分区可以依据须要启动调整和裁减,以顺应新发现的元素和更深化的钻研。
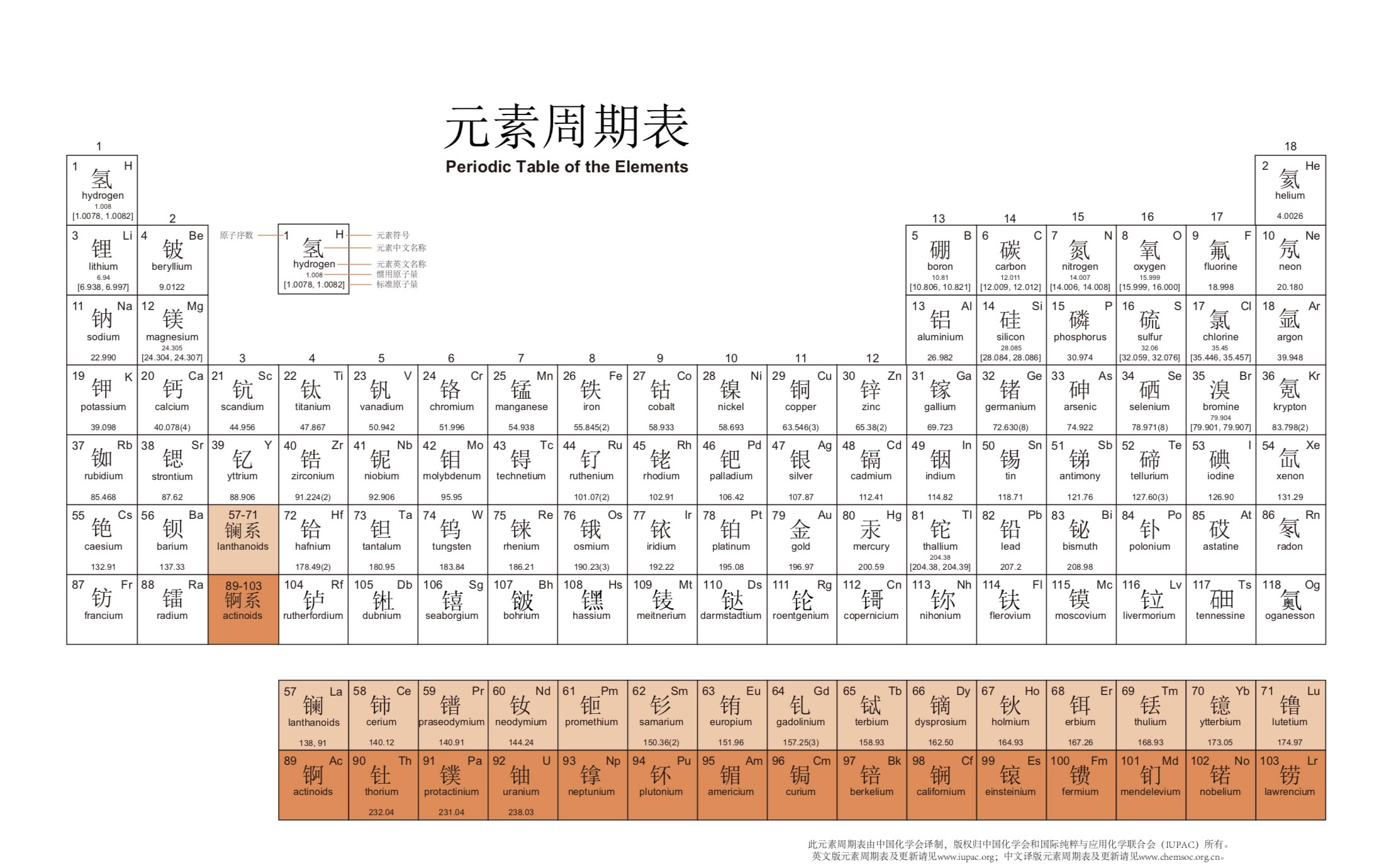
什么是元素周期表
元素周期表是一种以化学元素依照必定法令陈列的表格。
它将一切已知的化学元素依照原子序数(也称为元素序数或质子数)的顺序启动陈列,并依据元素的性质和特色启动分类。
元素周期表的最早版本由俄罗斯化学家门捷列夫于1869年提出,如今经常使用的是订正过的、蕴含118个已知元素的版本。
元素周期表依照水平行,称为周期,和垂直列,称为族(或组)启动组织。
基于元素周期表,咱们可以获取以下消息:
1. 元素符号,每个元素都有一个共同的符号,例如氢元素的符号为 H,氧元素的符号为 O。
2. 原子序数(元素序数),每个元素都有一个惟一的原子序数,示意元素核中的质子数。
原子序数为1的元素是氢,而原子序数为118的元素是奥气。
3. 原子量,元素周期表中给出的每个元素的原子量(相对原子品质),即元素原子的平均品质。
4. 元素性质,元素周期表将具备相似性质的元素放在一同。
例如,位于同一族的元素通常具备相似的化学性质和反响个性。
经过元素周期表,咱们可以更好地了解不同元素的性质、组成物质以及它们在化学反响和生命中的作用。
元素周期表是化学钻研、教育和通常中的基本工具之一。